|
Las Bandas de Hunter Schreger (BHS) representan estructuras del esmalte dental, originadas por la decusaciˇn de los haces de prismas que nacen en direcciones opuestas en el lÝmite amelodentinario (1). Este entrecruzamiento es regular, por lo que en cada banda se alternan zonas claras y oscuras. Los prismas, al presentar en cada hilera, anillo o plano, un transcurso ondulante, pueden ser seccionados transversalmente, dando origen a las bandas claras denominadas parazonas, o bien longitudinalmente dando lugar a la apariciˇn de las bandas oscuras o diazonas (Fig. 1). Algunos autores las consideran un fenˇmeno ˇptico debido al aspecto que presentan cuando son observadas en cortes por desgaste. En nuestras observaciones con lupa estereoscˇpica y microscopio ˇptico (Laboratorio de MicroscopÝa FOLP-UNLP) las bandas se evidencian como lÝneas claras y oscuras que se extienden desde el lÝmite con la dentina hacia la superficie externa, ocupando 4/5 del espesor del esmalte (Figs. 2 y 3). Generalmente adquieren una forma horizontal describiendo una leve concavidad hacia oclusal en las caras libres, y se disponen oblicuas ascendentes hacia oclusal.
 |
Figura 1. MicrografÝa del esmalte con bandas de hunter Schreger. Se observan zonas alternadas de prismas en secciˇn transversal y longitudinal produciendo un efecto de ondulaciones en la superficie del preparado. MEBx1000
|
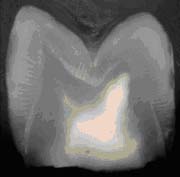 |
Figura 2. Corte longitudinal de un premolar superior visto con lupa estereoscˇpica. En las caras libres se observan bandas oscuras y claras alternadas de disposiciˇn horizontal.
|
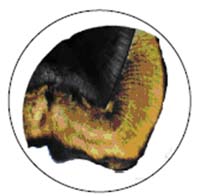 |
Figura 3. Preparado de una secciˇn longitudinal de la corona dentaria. MOx40
|
Existen discrepancias en la literatura sobre la naturaleza y comportamiento de las bandas de Hunter-Schreger. Osborn (2) demostrˇ mediante micro radiografÝas, grabado, pulido y tinciˇn, que las bandas no eran un fenˇmeno ˇptico sino que eran crestas y depresiones. La profundidad de esas depresiones aumentaba cuando el pulido final se realizaba despuÚs del uso de abrasivos gruesos sin pasar por grados intermedios. Braly A et al (3) consideran que la dureza del esmalte de molares humanos disminuye mßs del 50% desde la superficie oclusal hacia la uniˇn amelodentinaria. Algunos atribuyen esta caracterÝstica a un menor grado de mineralizaciˇn (4). Lynch et al. (5) estudiaron la implicancia de las bandas de Hunter- Schreger en la odontologÝa clÝnica y concluyeron que presentan ˇptima resistencia a la atriciˇn, abrasiˇn y fractura dentaria y favorecen la adhesiˇn en el esmalte.
Si bien las bandas no alcanzan la superficie del esmalte, los fenˇmenos de atriciˇn y desgaste pueden dejarlas expuestas a diferentes factores fÝsicos y quÝmicos de la cavidad bucal. Por lo tanto, nuestro propˇsito fue describir las variaciones en la dureza y en la composiciˇn elemental de las bandas de Hunter Schreger expuestas a una bebida sin alcohol.
MATERIALES Y M╔TODO
Se obtuvieron piezas dentarias extraÝdas por indicaciˇn con el correspondiente consentimiento informado del paciente. Se descontaminaron y se separˇ la porciˇn radicular. Se realizaron secciones vestÝbulo-linguales de las coronas que fueron incluidas en resina, desgastadas con papel de lija de granulaciˇn decreciente, pulidas a brillo espejo con suspensiˇn de al˙mina, lavadas con ultrasonido y secadas con calor seco. Las muestras se sumergieron en 100 ml de un agua natural saborizada durante 12 minutos.
Se realizaron registros de la composiciˇn quÝmica elemental del esmalte con BHS antes y despuÚs de la exposiciˇn a la bebida. El anßlisis elemental se realizˇ con un ESEM FEI Quanta 200 con sonda EDS (SeMFi-LIMF. FI- UNLP). Se obtuvieron espectros de energÝa dispersiva del calcio (Ca), fˇsforo (P) y se determinˇ la relaciˇn Ca/P. La dureza (H) se midiˇ con un nanoindentador TRIBOINDENTER HYSITRON (INTEMA-UNMdP).
La funciˇn de carga es un trapezoide bßsico de 4mN de carga mßxima, holding time de 2 seg, con tasas de carga y descarga de 800uN/seg. Se utilizˇ la prueba de t con un error aceptado de 0,05 y se determinˇ el porcentaje de reducciˇn de dureza mediante la fˇrmula: ΔHf=100*[(Hi-Hf)/Hi] donde Hi: dureza inicial; Hf: dureza final
RESULTADOS
El anßlisis quÝmico elemental determinˇ una variaciˇn en la relaciˇn calcio/fˇsforo despuÚs de la exposiciˇn a la bebida (Tabla 1). Los espectros Los espectros EDS del esmalte con bandas, sano y tratado presentan picos de calcio y fˇsforo evidentes por ser la composiciˇn principal del tejido adamantino.
TambiÚn aparecen otros elementos como cloro, sodio y magnesio en menor proporciˇn (Fig. 4 A y B).
Tabla 1. Valores porcentuales medios de calcio y fˇsforo del esmalte con bandas (expresados en peso%)
|
| Esmalte con Bandas Hunter Schreger Sano Tratado |
Sano |
Tratado |
| Calcio |
38,14▒1,17 |
39,39▒8,16 |
| Fˇsforo |
18,05▒0,5 |
19,56▒4,22 |
| Ca/P |
2,11▒ 0,02* |
2,00▒ 0,06* |
*La diferencia fue significativa (prueba de t, p<0,05)
A
|
B
|
 |
 |
| Figura 4. A Espectro EDS del esmalte sano. B espectro del esmalte expuesto a bebida |
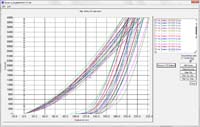
Con relaciˇn a la dureza superficial, el esmalte con bandas sano presentˇ un valor medio de 4, 24 GPa y despuÚs de la exposiciˇn a la bebida descendiˇ 1,54 GPa (Tabla 2). Las curvas representativas del esmalte sano y tratado se observan en la Figura 5 (A y B).
El porcentaje de reducciˇn de la dureza resultˇ del 62,56%.
Tabla 2. Valores de dureza H (GPa) en el esmalte con bandas
|
Esmalte BHS
|
Sano |
Tratado |
| Dureza H |
4,24▒ 0,43* |
1,54▒ 0,42*
|
*La diferencia fue significativa (prueba de t, p<0,05)
|
| A
|
 |
| B
|
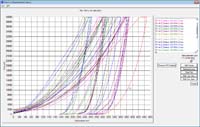 |
| Figura 5. Curvas de nanodureza. A esmalte sano, B despuÚs de la bebida. |
DISCUSIËN Y CONCLUSIONES
Distintos trabajos demuestran que las bandas de Hunter Schreger constituyen una forma particular de organizaciˇn de la microestructura del esmalte (6,7), aunque pocas veces son consideradas desde su importancia clÝnica.
El entrecruzamiento de los prismas origina que los cristales de hidroxiapatita se encuentren entre sÝ en ßngulos agudos resultando en un mayor de contenido de material orgßnico en esas regiones (8). Esta caracterÝstica podrÝa estar relacionada con la menor dureza descripta en la zona interna del esmalte (correspondiente al esmalte con bandas).
Jiang (9) destaca que el entrecruzamiento de prismas provee un mecanismo de detenciˇn de rajaduras, y potencia la resistencia a las fuerzas tensionales. No obstante, frente a las fuerzas de desgaste, las bandas presentan menor resistencia que el esmalte superficial radial.
En este estudio quedˇ demostrado que la exposiciˇn de las bandas a una bebida sin alcohol, provocˇ una importante disminuciˇn de la dureza superficial, reduciÚndose en mßs de la mitad con respecto al esmalte sano. Ademßs se determinˇ una pÚrdida de calcio, evidenciada en una menor relaciˇn calcio/fˇsforo despuÚs de la acciˇn de la bebida.
Estas variaciones fueron producidas por el contenido de acidulantes presentes en la composiciˇn de la bebida, que resultaron suficientes para producir desmineralizaciˇn a˙n en un tiempo breve como el del presente experimento (10).
Concluimos que esmalte BHS, resulta susceptible a las bebidas que contienen acidulantes, las cuales contribuyen a una disminuciˇn de las propiedades mecßnicas y desmineralizaciˇn por pÚrdida de calcio.
Estudios realizados con nanoindentation demostraron que la dureza y el mˇdulo de Young del esmalte de molares humanos disminuyen mßs del 50% desde la superficie oclusal hacia la uniˇn amelo-dentinaria en muestras de secciˇn transversal.
Posibles fuentes de estas variaciones son cambios en la composiciˇn quÝmica local, en la microestructura y en la orientaciˇn de los prismas.
Sin embargo, se demostrˇ que el impacto de la orientaciˇn del prisma en las propiedades mecßnicas medidas en escala de nanoidentaciˇn parece ser mÝnimo.
El esmalte tiende a clivarse a lo largo de las hileras de prismas, sin embargo, las las ondulaciones de los grupos de prismas se manifiestan como bandas de Hunter- Schreger que act˙an impidiendo el progreso de los planos de fractura.
Journal of Oral Rehabilitation 2011 38; 359ľ365
HunterľSchreger Band patterns and their implications for clinical dentistry
CD Lynch, VR OĺSullivan, P Dockery, CT Mcgillycuddy, JS Rees & A. J. Sloan
BIBLIOGRAF═A
1. Koenigswald W SP. Tooth enamel microstructure Koenigswald W SP, editor. Rotterdam: Balkema; 1997. pp. 277-280
2. Osborn, JW. The nature of the Hunter- Schreger Bands in Enamel Arch. Oral Biol. 1965 Vol 10, pp. 929-933
3. Braly A; Darnell LA; Mann AB; Teaford MF; Weihs TP The effect of prism orientation on the indentation testing of human molar enamel. Arch Oral Biol. 2007 Sep;52(9):856-60
4. Gˇmez de Ferraris ME; Campos Mu˝oz A (2009) HistologÝa, embriologÝa e ingenierÝa tisular bucodental. 3 ed. MÚdica Panamericana, 2009
5. Lynch, CD; O┤Sullivan, VR; Dockery, P; McGillycuddy, CT; Rees, JS; Sloan, AJ. Hunter- Schreger Bands patterns and their implications for clinical dentistry J. Oral Rehabil. 2010 38 (5): 359-65
6. Goin, F; et al. Microestructura del esmalte dentario: definiciones y conceptos R.A.O.A. Buenos Aires, 2007 Vol. 95 N░5, oct- dic, pp. 393-398
7. Rensberger, J. Mechanicals adaptation in enamel en: Tooth enamel microstructure, Koenigswald, W; Sander, P (eds.) Balkema, Rotterdam, 1997 pp 237-257
8. Nancy, A. Ten Cate┤s Oral Histology,Development, Structure and Function. St. Louis, Mo USA The C.V. Mosby Comp .2003 6th ed.
9. Jiang Y; Spears, IR; Macho, GA. An investigation into fractured surfaces of enamel of modern human teeth: a combined SEM and computer visualization study Archs. Oral Biol. 2003 48: 449-457
10. Ehlen Leslie A, Marshall Teresa A, Qian Fang, Wefel James S, Warren John J. Acidic beverages increase the risk of in vitro tooth erosion. Nutr Res. 2008; 28(5): 299-303.
|
